3D 프린팅 잉크와 줄기세포를 활용한 인공 심장 개발의 현황 (The Frontier of Artificial Cardiac Development Using 3D Printing Ink and Stem Cells)
바이오융합공학전공 이길용 교수
1. 서론 (introduction)
3D 프린팅 기술은 최근 제조업, 건축, 항공우주 산업 등 광범위한 분야에서 큰 변화를 이끌었습니다. 이 중에서도 특히 의료 분야에서의 그 영향력은 매우 두드러지며, 맞춤형 의료 솔루션의 개발, 질병 진단 및 치료 방법의 혁신, 그리고 인공 장기 제작에 이르기까지 다양한 응용 분야에서 그 가능성을 입증하고 있습니다. 인공 장기 개발 분야에서 3D 프린팅 기술, 특히 바이오프린팅 기술은 신체 조직과 유사한 구조를 만들어낼 수 있는 가능성으로 인해 많은 주목을 받고 있습니다. 이 3D바이오 프린팅 기술로 도래 되는 인공장기 제작은 장기 기증과 관련된 제약을 극복하고, 맞춤형 치료법을 제공하여 환자의 삶의 질을 개선할 수 있는 엄청난 잠재력을 가지고 있습니다.
3D바이오프린팅은 생체 호환성이 높은 재료로 만들어진 바이오잉크를 사용하여 세포, 단백질 및 기타 생물학적 요소들을 층층이 쌓아 올려 실제 인체 조직과 유사한 구조를 만들어냅니다. 이 과정에서 중요한 것은 바이오잉크의 선택입니다. 바이오잉크는 세포의 생존과 성장, 그리고 조직 형성에 필수적인 환경을 제공해야 하며, 동시에 인쇄 과정에서 안정적인 구조를 유지할 수 있는 기계적 특성도 가져야 합니다. 전 세계 연구자들은 다양한 자연적 또는 합성 재료를 바탕으로 한 바이오잉크를 실험하고 있으며, 이 잉크들은 세포를 지지하고, 세포에 영양분을 제공하며, 적절한 세포 간 상호작용을 촉진하는 등의 다양한 역할을 합니다.
하지만 3D 프린팅을 이용한 인공 장기 개발은 단순히 바이오잉크를 선택하고 인쇄하는 것 이상의 복잡한 과정을 포함합니다. 이 기술은 세포 생물학, 재료 과학, 기계 공학, 컴퓨터 과학 등 다양한 분야의 지식과 기술이 통합된 결과이며, 해당 분야의 전문가들의 활발한 연구가 진행중입니다. 세포를 적절한 위치에 정밀하게 배치하고, 생체 구조와 기능을 반영하여야 하며, 복잡한 인체 조직의 3차원 구조를 성공적으로 재현하기 위해서는 고도의 설계와 계획, 그리고 테스트가 필요합니다.
더 나아가, 인공 장기가 실제 임상에서 사용되기 위해서는 생체 호환성, 장기 기능성, 안전성 등 여러 면에서 철저한 검증이 이루어져야 합니다. 이는 장기의 생존 기간, 기능 유지, 면역 반응 등을 포함한 다양한 요소를 고려해야 하는 매우 복잡한 과정입니다. 따라서 임상 적용을 위해서는 장기의 장기간 생존과 기능을 검증하는 임상 시험, 그리고 규제 기관의 승인이 필요합니다.
이처럼 3D 프린팅을 이용한 인공 장기 개발은 매우 복잡하고 다학제적인 분야이며, 아직 많은 연구와 발전이 필요한 상태입니다. 하지만 이 기술이 가지고 있는 잠재력은 무궁무진하며, 앞으로 수십 년 동안 의료 분야에서 가장 주목받는 것으로 예상됩니다. 관련 연구의 진전과 함께, 이 기술은 장기 이식을 필요로 하는 환자들에게 새로운 희망을 제공하고, 맞춤형 의료 솔루션의 발전을 촉진하여 전반적인 의료 서비스의 질을 개선할 것으로 기대됩니다.
3D 프린팅 잉크를 활용한 인공장기 개발에서 줄기세포와 바이오잉크의 중요성은 상당하며, 이 두 요소는 현대 조직 공학과 장기 재생 분야에서 중추적인 역할을 하고 있습니다.
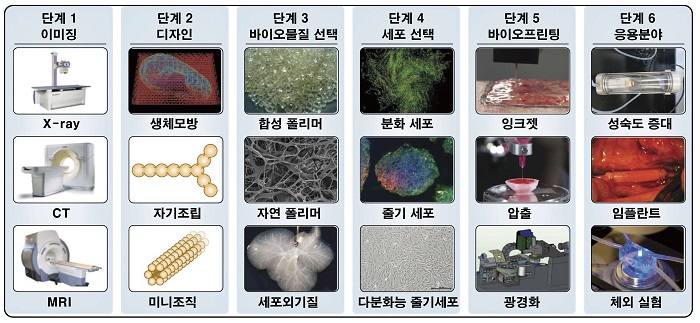
Figure 1. 3D 조직 바이오 프린팅을 위한 일반 적인 과정. 단계1. 바이오 프린팅된 조직의 디자인을 구축하는데 필요한, 손상된 조직과 그 환경의 이미징. 단계2. 생체 모방, 조직 자체 조립 및 미니 조직 빌딩 블록을 단독 또는 다양한 조합을 통한 조직 디자인. 단계3,4. 조직의 형태와 기능에 필수적인 생체재료와 세포의 선택. 일반적으로 해당 재료에는 합성 또는 자연 폴리머와 탈세포화 세포외기질이 포함됨. 단계 5. 이러한 구성 요소는 잉크젯, 마이크로 압출 또는 광경화 보조 프린터와 같은 바이오 프린팅 시스템과 통합되어 프린팅. 단계 6. 일부 조직은 이식 전에 성숙 기간이 필요하며, 대안적으로 3D 조직은 신약개발 및 개인화약물을 개발을 위한 체외 진단을 응용을 위해 사용될 수 있음 (1).
2. 줄기세포 (Stem cells)
세포 기반 인공 심장 제작에서 줄기세포의 역할은 매우 중요하며, 재생 의학 및 조직 공학의 혁신적인 발전을 가능하게 할 수 있습니다. 줄기세포는 다양한 심장 세포 유형으로 분화할 수 있는 능력을 가지고 있으며, 이는 심장 조직의 복잡한 구조를 재현하기 위해 필수적입니다. 환자의 체세포로부터 유도된 iPSCs는 환자 특유의 유전적 및 생물학적 특성을 가지고 있어, 제작된 인공 심장이 환자의 신체와 더 잘 호환될 가능성을 높이고, 이식 후 거부 반응과 합병증의 위험을 감소시킬 수 있습니다. 또한, 줄기세포는 자가 복구 및 재생 능력을 가지고 있어, 인공 심장 내에서의 세포 손상이나 기능 손실을 보완할 수 있으며, 이는 인공 심장의 수명과 기능을 향상시킬 수 있습니다. 3D 바이오 프린팅 기술과 결합하여, 줄기세포는 정밀하게 설계된 심장 조직을 형성하는 데 사용될 수 있으며, 이 과정에서는 줄기세포가 적절한 구조와 환경에 배치되어 자라나며, 최종적으로 기능하는 심장 조직을 형성하게 됩니다.
줄기세포로부터 유도된 심장 세포는 질병 모델을 구축하고 신약의 효과 및 안전성을 평가하는 데 사용될 수 있습니다. 이는 특히 심장 질환의 병리를 이해하고 새로운 치료법을 개발하는 데 중요합니다. 또한, 유도 만능성 줄기세포(iPSCs)의 사용은 윤리적 논란이 적고, 환자 자신의 세포로부터 쉽게 얻을 수 있어, 심장 조직 공학에 있어 선호되는 세포 소스가 되고 있습니다.
신약 개발 관점에서 동물 모델은 다양한 질병의 검증에 중요한 역할을 해왔습니다. 모든 안전성 및 효능 매개변수는 사람 대상 첫 임상 시험 시작 전에 동물에서 계속 테스트됩니다. 하지만, 연구 및 약물 개발에서 동물 모델의 중요성에도 불구하고, 동물과 인간의 생리 및 병리 생리학 사이의 불일치는 임상 연구에서 80% 이상의 약물테스트를 통과하지 못하고 있습니다. 따라서 동물 모델은 인간 체계에 존재하는 복잡성이나 병리학적 다양성을 반영하는 데 실패했으며, 이는 임상 성공을 제한하고 있습니다. 배아 발달 중에는 인간과 동물 사이에서 조직 형태 생성의 패턴과 시기에 현저한 차이가 있습니다. 예를 들어, 쥐와 인간 사이의 줄기 세포 표면 마커 집합체의 차이는 세포 조직의 운동성과 증식에서 주요 차이를 야기합니다. 따라서 인간 모델 사용이 인간의 장애 대한 분자생물학적 메커니즘을 밝히고 대상 치료법 개발에 있어 더 신뢰성 있게 여겨지고 있습니다.
다기능성 줄기세포(pluripotent stem cells, PSCs), 예를 들어 인간 내세포질 배아줄기세포(embryonic stem cells, ESCs)와 유도만능성 줄기세포(induced pluripotent stem cells, iPSCs)의 발견은 인간 다양한 장기의 형성과 선천성 및 성숙한 심장 질환의 기반을 연구하는데 혁명적인 도구로 등장했습니다. 특히, iPSC 기술은 윤리적인 문제를 해결하여 더욱 정확한 질병 모델링 플랫폼을 개발하는 데 기여했습니다. 또한, iPSC에서 유래된 다양한 세포(iPSC-CMs)와 유전체 편집 접근법을 사용하여 다수의 단일유전질 및 복잡한 병리학이 체외 (in-vitro)에서 연구되어, 질병 메커니즘에 대한 새로운 관점을 제공하고 있습니다. 특히, 심장부분의 iPSC에서 유래한 세포 유형, 예를 들어 iPSC에서 유래된 내피세포(iPSC-ECs), iPSC에서 유래된 심장 섬유아세포(iPSC-CFs), 그리고 iPSC에서 유래된 평활근세포(iPSC-SMCs)의 사용은 심장 모델의 세포 다양성을 크게 풍부하게 하며, 성인 심장과 같은 특성의 생리학적 성숙과 재현이 가능합니다.
줄기세포를 활용한 세포 기반 인공 심장 제작은 여전히 활발한 연구가 진행 중인 분야이며, 이 기술이 임상에 적용되기까지는 여러 과학적, 기술적, 규제적 장벽을 극복해야 합니다. 하지만, 그 잠재력은 엄청나며, 향후 심장 질환 치료에 혁명을 가져올 수 있는 가능성을 지니고 있습니다.
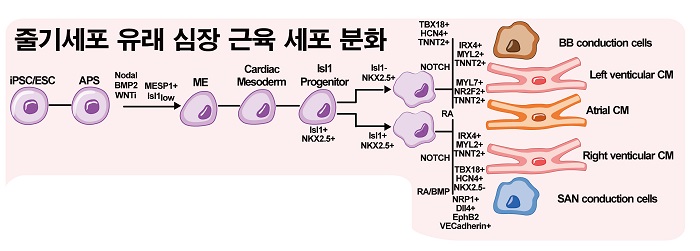
Figure 2 다기능성 줄기세포 (IPSC) 심장 세포로 유도하기 위한 세포 분화 방식. 특정 세포 형태 발생 및 그 정체성을 유도하는 주요 요인은 발달 경로 (세포 신호)에 표시하였음. 대부분의 경우, 모든 심장 세포 하위 유형은 줄기세포에서 발생하는 중배엽내피 조상 세포(KDR [kinase insert domain receptor] 및 MESP1 [mesodermal posterior 1])에서 기원함. 이후 Wnt 조절은 심근세포(CMs), 내피를 생성하는 데 이르게 하며, 특정 심실의 근육세포 유형은 골 형성 단백질(BMP)과 레티노산(RA) 매개 NOTCH 신호 활성화를 통해 얻어지며, 평활근 세포와 주위 세포는 측판 중배엽(LPM)과 축배엽(PM)에서 발달함. 심장의 섬유아세포는 심장 외피와 중배엽 조상 세포에서 유래하며, APS는 전방 원시 줄기를 나타내며; ESC는 배아줄기세포; ETV2는 ets 변형 전사 인자 2; FGF는 섬유아세포 성장 인자; IFN은 인터페론; IL은 인터류킨; SAN은 방실결절; TPO는 혈소판 생성 인자; VEGF는 혈관 내피 성장 인자를 나타냄 (2).
3. 바이오 잉크 (Bio-ink)
줄기세포 기반 3D 바이오 잉크 개발은 현대의 조직 공학과 재생 의학에서 가장 앞선 연구 분야입니다. 이 기술은 인간 조직과 장기를 모방하고 재생하는 데 필수적인, 혁신적이고 복잡한 과정을 포함하고 있습니다. 세포 기반 인공 심장 제작을 위한 바이오잉크의 역할은 매우 중요하며, 다차원적인 접근을 필요로 합니다. 바이오잉크는 세포를 특정 위치에 정밀하게 배치하고, 심장 조직의 복잡한 3차원 구조를 형성하는데 사용됩니다. 이는 심장의 다양한 기능적 영역을 모방하는 복잡한 조직을 구축하는 데 필수적입니다. 제공하는 생체 호환성 환경은 세포의 생존, 성장, 분화를 촉진하여 자연스러운 상태에서 심장 세포가 기능을 수행하도록 지원하며, 이는 인공 심장의 전반적인 기능성과 수명에 영향을 미칩니다.
또한, 바이오잉크는 인쇄 과정에서 안정적인 구조를 유지하며, 인공 심장이 실제 심장과 유사한 기계적 강도와 탄력성을 가질 수 있도록 하는 기계적 속성을 조절할 수 있게 합니다. 이는 심장의 전기적 특성과 혈류 동력학을 모방하는 생물학적 신호를 제공하는 데도 중요하며, 이러한 멀티셀룰러 (multi-cellular) 시스템의 구축은 심장의 복잡한 기능을 더 정확하게 모방하며, 질병 모델링 및 약물 반응 테스트에도 사용될 수 있어, 심장 질환의 병리학적 특징을 모방하고 신약의 효능과 독성을 효과적으로 평가할 수 있습니다.
바이오잉크의 지속적인 개발과 혁신은 심장 조직 공학의 중심에 서 있으며, 생체 호환성, 기계적 특성, 세포 지지 능력 등을 최적화하기 위해 다양한 종류의 바이오잉크가 개발되고 있습니다. 이러한 연구와 발전은 심장 질환 치료와 재생 의학에 중요한 진보를 가져올 것으로 기대되며, 미래의 의료 혁신에 중요한 기여를 할 것입니다. 바이오잉크는 또한 다양한 세포 유형과 조직의 복잡한 상호작용을 지원하기 위해 다양한 화학적 구성과 물리적 특성을 가질 수 있어야 합니다. 이는 심장의 복잡한 생리학적 및 기능적 요구를 충족하는 것을 목표로 합니다. 심장 조직의 다양한 부분, 예를 들어 심근, 심장 판막, 관상 동맥 등은 서로 다른 기계적 강성과 생물학적 신호가 필요하며, 바이오잉크는 이러한 요구를 만족시킬 수 있어야 합니다.
더불어, 바이오잉크의 발전은 또한 체외에서의 심장 조직 배양과 관련된 기술적 도전을 극복하는 데 중요합니다. 세포가 적절하게 분화하고 성숙하여 실제 심장 조직과 유사한 기능을 수행하도록 하기 위해서는, 바이오잉크 내에서의 적절한 세포 배치, 영양 공급, 산소 전달 및 폐기물 제거 등의 문제를 해결해야 합니다. 이러한 조건을 충족시키는 바이오잉크의 개발은 심장 조직 공학의 성공에 결정적입니다. 바이오잉크는 세포 기반 인공 심장 제작에 있어 필수적인 구성 요소로, 그 기능과 발전은 심장 조직의 성공적인 재현과 임상적 적용 가능성에 직접적인 영향을 미칩니다. 이 분야의 지속적인 연구와 개발은 향후 인공 심장 제작의 효율성과 효과를 크게 향상시킬 것으로 기대됩니다.
4. 3D 프린팅 및 잉크 기반 심장 조직 개발 (세종대학교-하버드대학교 공동연구)
심장 조직 내의 세포 내부 및 세포 간 조직은 조정된 전기기계적 결합과 심장의 효율적인 근육 수축을 촉진하는 데 도움을 줍니다. 이러한 조직된 구조를 달성하기 위해, 세포 외 기질(ECM) 단백질은 세포에 대한 위상적 및 생화학적 신호로 작용하며, 이는 조직 발달에 중요합니다. 이는 특히 심장에서 중요한데, 여기서 심장 조직의 계층적 조직이 필요하여 여기서는 흥분-수축 결합의 시공간 역학을 조절하고, 이로 인해 심장 주기가 발생합니다. 심장의 구조-기능 관계를 체외에서 재현하는 것은 상당한 도전을 나타냅니다. 이는 세포 규모와 거시적 장기 수준에서 조직 자체 조직화를 통제하는 것을 요구합니다. 심장 세포 조직을 복제하기 위한 노력으로, 연구자들은 마이크로 접촉 인쇄, 광리소그래피, 방향성 동결 건조, 섬유 스피닝 및 마이크로 생리학적 칩 제작을 통해 생체 고분자와 하이드로젤을 공학적으로 개발했습니다. 그러나 이러한 방법들은 복잡한 기하학을 가진 조직을 생산하는 능력이 제한되어 있으며, 심장 기능을 완전히 복제하는 데 한계가 있습니다. 특히, 3차원(3D) 기하학을 모방하는 장기 모델을 구축하기 위해서는 첨가제 제조 전략이 필요합니다.
특히, 3D 프린팅은 조직 모델을 공학하기 위해 점점 더 사용되고 있으며, 이는 인쇄 전에 3D 구조를 쉽게 디자인하고 편집할 수 있게 하고, 유연한 바이오 재료 잉크의 조성으로 복잡한 3D 구조를 제작할 수 있게 합니다. 이를 위해, 하이드로젤 기반 잉크나 인쇄 기술을 개발하기 위한 상당한 노력이 이루어졌습니다. 이러한 노력에는 복합 노즐 시스템을 사용한 다재료 잉크 인쇄, 광경화성 하이드로젤 인쇄, 점증제 추가 또는 희생지지재료 인쇄 등 3D 안정성과 형태 충실도를 향상시키는 것이 포함됩니다. 그러나 이러한 노력은 조직 자체 조직화와 정렬에 대한 제한된 통제를 제공합니다. 그 결과, 마이크로미터와 나노미터 규모에서 센티미터 규모로의 규모를 연결하여 공학적 심장 모델 내부의 세포 내부 및 세포 간 조직화를 유도하는 것은 기능성 장기 및 조직의 3D 프린팅에서 주요한 도전 과제로 남아 있습니다.
최근, 세종대학교와 하버드대학교와 공동연구를 통하여, 사전 제작된 미세 규모 섬유를 포함하는 3D 지지체를 인쇄하는 것이 심근세포가 심장 방을 형성하기 위해 자체 조직화할 수 있는 자기 지지형 지지체를 제공할 것이라고 가설을 세우고, 심장의 세포 외 기질(ECM) 네트워크에서 영감을 받아, 젤라틴 섬유를 젤라틴과 알지네이트(Gel-Alg) 하이드로젤 매트릭스에 주입하여 우리의 잉크를 설계했습니다 (그림 3). 셀룰로오스 나노섬유와 탄소 나노튜브와 같이 이전에 잉크에서 사용된 것과는 달리, 세포외기질 중 하나인 피브로넥틴(Fibronection)이 코팅된 젤라틴 섬유는 매트릭스-세포 부착을 촉진하는 아르기닌-글리신-아스파트산(RGD) 펩타이드 결합 도메인을 포함합니다. 또한, 나노 미세 섬유를 하이드로젤에 포함함으로써 잉크의 유변학적 성질을 변경하여, 지지 구조나 재료 없이도 정확하고 복잡한 3D 지지체를 만들 수 있었습니다. 본 연구진은 위상적 및 화학적 신호를 정렬된 젤라틴 미세섬유의 형태로 통합함으로써, 이런 방식으로 인쇄된 3D 심실 지지체가 심근세포의 이방성 근육 조직으로의 자체 조직화를 촉진할 것 하였습니다 (그림3).
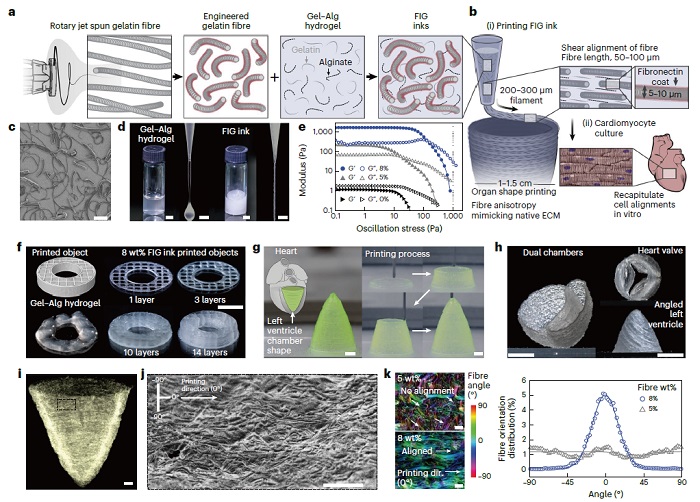
Figure 3. 3D 프린트 된 조직 지지체에 대한 바이오 잉크. (a) 나노 섬유가 포함된 잉크 구성 요소 제작 방법. 파편화된 젤라틴 나노 섬유가 젤라틴-알지네이트 하이드로젤과 결합될 때 (빨강색은 세포외기질), 잉크 점도가 증가하며 고체 같은 행동을 나타내어, 계층적 구조를 가진 심실 지지체의 3D 프린팅을 가능함. (b) 3D 프린팅 도중에 나노 섬유 정렬은 3D 지지체에서 실제 ECM과 유사한 이방성 구조적 특징을 유도하여, 체내 심장 근육을 재현하기 위한 조직 정렬 및 조직화를 촉진. (c) 젤라틴 나노 섬유를 보여주는 주사 전자 현미경 이미지. 100 μm. (d) 바이오잉크에 나노 섬유가 포함되었을 떄 물성 비교. 나노 섬유가 포함되지 않았을 때는 프린팅이 불가능 한 낮은 점도의 액체 같은 행동을 나타냄. (e) 바이오 잉크의 물성 테스트, 농도 의존적이고 변형 의존적인 전단 액화 행동 및 솔-젤 전환을 나타냄. (f) 3D 도넛 형태의 프린팅 테스트5 mm. (g) 3D 프린팅을 통한 심장의 왼쪽 심실의 원추형 모델. 2 mm. (h) 3D 프린팅을 통한 주변 방향으로 인쇄된 자기 지지식 이중 심실 챔버와 심장 판막 및 대각선 (30°) 으로 기울어진 왼쪽 심실. (i) 3d프린트된 심실 지지체의 마이크로 컴퓨터 단층촬영 이미지로, 3D 프린트된 형상에서의 섬유 구조를 나타냄, 1 mm. (j) 3D 프린트된 심실 지지체의 주사 전자 현미경 이미지로 인쇄 방향의 섬유 정렬을 나타냄, 200 μm. k, 5 와 8 wt% 나노 섬유를 가진 3D 프린트된 심실 지지체의 공초점 이미지에서 섬유 정렬 분석, 그리고 해당 섬유 방향 각도 분포 그래프; 0°는 인쇄 방향(dir.)을 나타냄, 100 μm. (3)
5. 결론 및 향후 연구방향
3D 프린팅 잉크를 활용한 줄기세포 기반 인공 심장 개발은 의학과 생명 공학의 중요한 전진 영역이며, 연구의 방향을 설정함에 있어 다음과 같은 중요한 분야에 집중을 요구 합니다. 첫째, 바이오잉크의 고도화에 주목해야 합니다. 심장 조직의 복잡한 구조와 기능을 더욱 정확하게 모방하기 위해, 바이오잉크의 생체 호환성, 기계적 특성, 생물학적 기능을 개선하는 연구를 추진해야 합니다. 이는 재료 과학, 생화학, 세포 생물학 등 다양한 분야의 지식을 통합하고 새로운 소재와 기술을 탐색하는 데 기여할 수 있는 기회입니다. 둘째, 세포 분화 및 조직화 기술의 발전을 추구해야 합니다. 줄기세포가 특정 심장 세포 유형으로 효과적으로 분화하고 적절하게 조직화되어 실제 심장처럼 기능할 수 있도록 하는 기술의 발전이 필요합니다. 이는 세포 생물학, 생체 공학, 조직 공학의 교차점에 있으며, 여러분이 창의적이고 혁신적인 실험 설계와 분석을 통해 기여할 수 있는 분야입니다. 셋째, 인공 심장의 통합 및 시스템화에 대한 연구가 중요합니다. 심장의 다양한 기능적 측면을 모방하고 실제 생리적 조건에서의 성능을 평가하기 위해, 다양한 세포 유형, 신호 전달 경로, 그리고 기계적 구조를 포함하는 완전한 인공 심장 시스템의 개발을 추진해야 합니다. 이는 복잡한 시스템을 이해하고, 실제 적용 가능한 솔루션을 개발하는 데 중점을 둔 연구로 이어질 것입니다. 넷째, 인공 심장의 안전성과 효능을 평가하는 연구를 진행해야 합니다. 이는 임상적 적용 전에 필수적인 단계로, 잠재적인 부작용, 거부 반응, 장기간 기능 유지 등을 포함합니다. 임상 연구, 생물 통계학, 의료 윤리 등 다양한 분야의 전문 지식을 발휘할 수 있는 영역입니다. 다섯째, 줄기세포 기반 인공 심장 개발과 관련된 윤리적, 법적, 규제적 문제를 해결하기 위한 지속적인 연구가 필요합니다. 이는 학제간 협력과 깊은 윤리적 고민을 요구하는 분야로, 사회적, 법적, 윤리적 측면에서의 중요한 의사 결정에 참여할 수 있습니다. 마지막으로, 개인화된 치료법으로의 확장에 대한 연구를 강조해야 합니다. 각 환자의 유전적 및 생물학적 특성을 고려하여 개인의 심장 질환의 특성에 더 잘 맞는 맞춤형 인공 심장을 제작할 수 있는 방법에 대한 연구가 필요합니다. 이는 정밀 의료의 전망을 향상시키고, 환자 맞춤형 해결책을 제공하는 데 기여할 것입니다. 이러한 연구 방향들은 줄기세포 기반 인공 심장 개발의 효과적인 진전을 위해 필수적이며, 여러분의 지식, 기술, 창의력을 발휘하여 심장 질환의 치료와 관리에 혁명을 가져올 잠재력을 가지고 있습니다. 본 연구실은 해당 연구와 혁신이 이 분야에서 집중에서 연구를 하고 있으며 중요한 발전을 이루기를 기대하고 있습니다.
참고문헌
1. S. V. Murphy, A. Atala, 3D bioprinting of tissues and organs. Nat Biotechnol 32, 773-785 (2014).
2. D. Thomas, S. Choi, C. Alamana, K. K. Parker, J. C. Wu, Cellular and Engineered Organoids for Cardiovascular Models. Circ Res 130, 1780-1802 (2022).
3. S. Choi et al., Fibre-infused gel scaffolds guide cardiomyocyte alignment in 3D-printed ventricles. Nature Materials, (2023).
4. K. Y. Lee et al., An autonomously swimming biohybrid fish designed with human cardiac biophysics. Science 375, 639-647 (2022).
5. H. Chang et al., Recreating the heart's helical structure-function relationship with focused rotary jet spinning. Science 377, 180-185 (2022).
6. A. Lee et al., 3D bioprinting of collagen to rebuild components of the human heart. Science 365, 482-487 (2019).
7. S. J. Park et al., Insights Into the Pathogenesis of Catecholaminergic Polymorphic Ventricular Tachycardia From Engineered Human Heart Tissue. Circulation 140, 390-404 (2019).